CRISPR: a tesoura genética que está reescrevendo o futuro da biotecnologia
A tecnologia que edita DNA de forma rápida, precisa e relativamente barata.
CRISPR: a tesoura genética que está reescrevendo o futuro da biotecnologia
A tecnologia CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats) revolucionou a biologia ao permitir editar o DNA de forma rápida, precisa e relativamente barata , algo que parecia ficção científica até poucos anos atrás. Hoje, ela está abrindo caminho para curas de doenças genéticas, novas terapias contra o câncer, plantas mais resistentes e até debates éticos sobre edição de embriões humanos.
Origem: de um mecanismo bacteriano à revolução genética
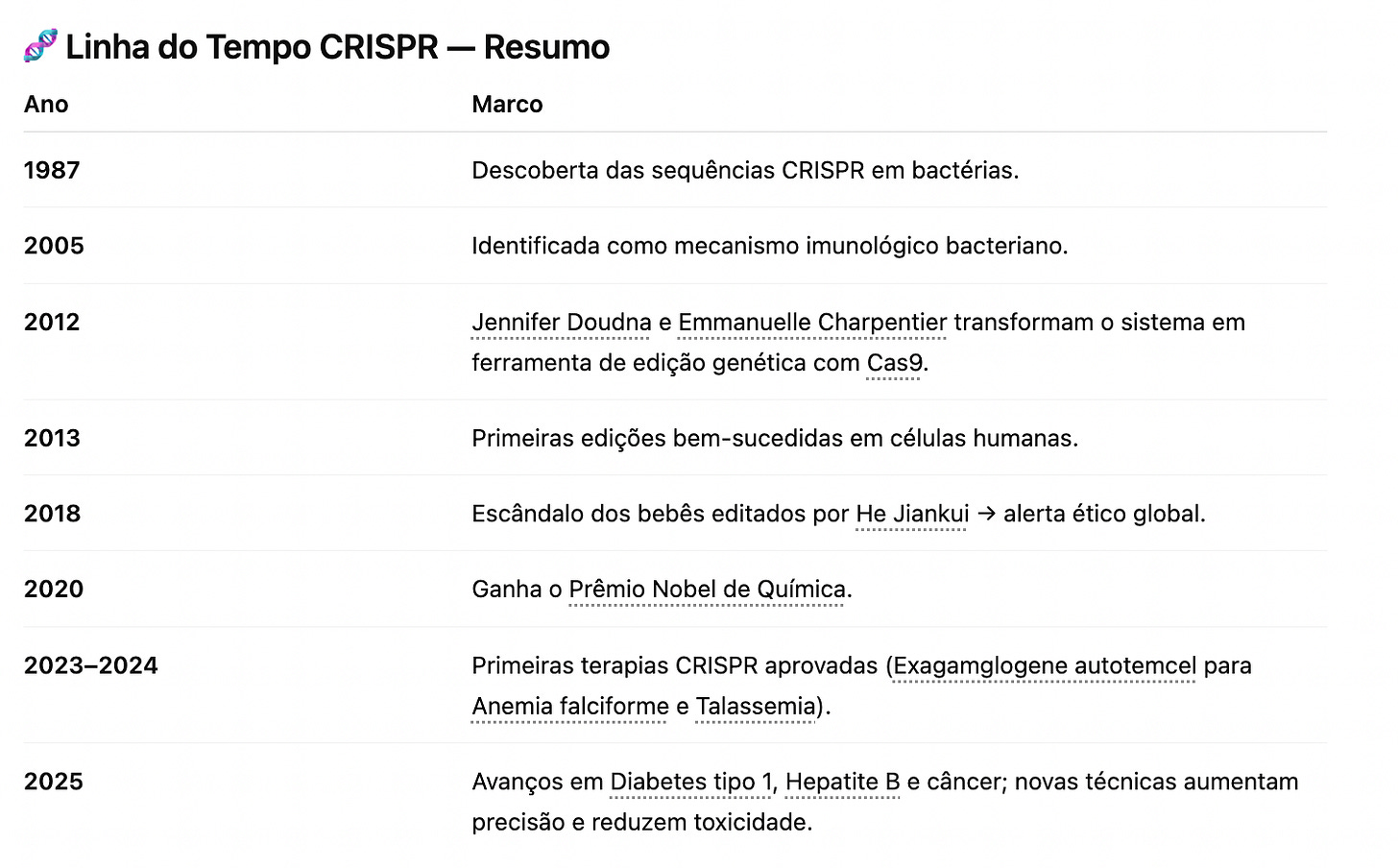
O sistema CRISPR foi identificado pela primeira vez em 1987 por cientistas japoneses que notaram sequências de DNA repetidas em bactérias, mas sem compreender sua função. Em 2005, descobriu-se que essas sequências funcionavam como um sistema imunológico adaptativo das bactérias, que as protege de vírus armazenando fragmentos do DNA viral.
O grande salto veio em 2012, quando Jennifer Doudna e Emmanuelle Charpentier demonstraram que a proteína Cas9 poderia ser guiada por um RNA sintético para cortar DNA em pontos específicos. Isso transformou o mecanismo bacteriano em uma ferramenta de edição genética universal, valendo-lhes o Prêmio Nobel de Química de 2020.
Como o CRISPR funciona
Em termos simples, o CRISPR funciona como uma “tesoura molecular”:
Um RNA-guia é projetado para se encaixar exatamente na sequência de DNA alvo.
A enzima Cas (como a Cas9) corta o DNA nesse ponto preciso.
As células então reparam o DNA, podendo inserir, apagar ou substituir genes no processo.
Esse método é muito mais simples e barato que as técnicas anteriores de edição genética (como TALENs e ZFNs), o que democratizou a engenharia genética em laboratórios no mundo todo.
Por que o CRISPR é importante
Medicina personalizada: possibilita terapias sob medida para doenças genéticas raras e comuns, como Anemia falciforme, Fibrose cística e Diabetes tipo 1.
Câncer e doenças virais: permite editar células do sistema imunológico para atacar tumores ou vírus como HIV e Hepatite B.
Agricultura de precisão: gera plantas mais resistentes a pragas, à seca e ao calor, e com maior valor nutricional.
Ciência básica e biologia sintética: acelera a pesquisa de genes e abre caminho para a criação de organismos com novas funções.
Em resumo, o CRISPR reduz anos de trabalho para semanas, e milhões de dólares para milhares — alterando a escala do que é possível fazer na biotecnologia.
Avanços recentes (agosto–setembro de 2025)
Tratamento de Diabetes tipo 1 com células editadas
Cientistas implantaram células pancreáticas humanas modificadas com CRISPR para produzir insulina em pacientes, sem necessidade de imunossupressores , algo inédito.Terapia para Hepatite B (HBV)
A empresa Excision BioTherapeutics apresentou resultados pré-clínicos do candidato EBT-107, que remove o DNA do vírus HBV do fígado e impede novas integrações virais.Entrega mais eficiente e menos tóxica
Pesquisadores da Northwestern University criaram nanopartículas envoltas em DNA que aumentam em até 3 vezes a eficiência do CRISPR e reduzem os efeitos tóxicos da entrega celular.Edição de mutações do gene KRAS em Câncer de pulmão
Equipes espanholas desenvolveram um sistema CRISPR de alta precisão que distingue mutações específicas (G12C e G12D) com menos efeitos colaterais fora do alvo.Investimentos e fusões
Empresas de biotecnologia como YolTech Therapeutics e Integra Therapeutics captaram dezenas de milhões para desenvolver terapias CRISPR in vivo. A Eli Lilly anunciou aquisição da Verve Therapeutics por até US$ 1,3 bilhões, reforçando o apetite do setor.Polêmicas Éticas e Sociais
Edição de embriões humanos (linha germinativa)
Caso emblemático: He Jiankui (2018) anunciou o nascimento de bebês geneticamente editados para serem resistentes ao HIV.
Gerou indignação global porque alterações na linha germinativa são herdáveis por futuras gerações e seus efeitos de longo prazo são desconhecidos.
Vários cientistas defendem um moratório internacional de 10 anos para esse tipo de experimento.
Desigualdade de acesso e “engenharia social genética”
Tratamentos CRISPR atuais podem custar mais de US$ 2 milhões por paciente, o que pode aprofundar desigualdades e criar um mercado para “melhorias genéticas” acessíveis só a elites.
Há receios de que, no futuro, isso gere uma divisão entre “geneticamente otimizados” e “não editados”.
Consentimento e direitos dos pacientes
Muitos ensaios envolvem crianças ou populações vulneráveis, levantando dúvidas sobre consentimento informado adequado e sobre exploração biomédica.
Polêmicas Legais e Regulatórias
Disputas de patentes
Conflito entre University of California/University of Vienna e Broad Institute sobre quem detém os direitos da invenção do CRISPR-Cas9.
Litígios continuam até 2025 e afetam licenciamento, royalties e preço de terapias.
Falta de normas globais
Não há consenso internacional sobre até onde a edição genética pode ir. Alguns países permitem testes clínicos, outros proíbem completamente, criando “turismo genético” para contornar restrições legais.
Polêmicas Ambientais e de Biossegurança
Liberação de organismos editados no meio ambiente
Projetos que usam CRISPR para modificar mosquitos transmissores de Malária ou plantas resistentes a pragas podem ter efeitos ecológicos imprevisíveis e irreversíveis.
Há medo de “gene drives” fora de controle, que poderiam se espalhar e alterar ecossistemas inteiros.
Possível uso bélico ou bioterrorista
CRISPR é simples e barato o suficiente para ser usado fora de laboratórios regulados. Há temores de que possa ser explorado para criar armas biológicas ou patógenos sintéticos.
No Brasil.
Pesquisas e laboratórios ativos
Embrapa (Empresa Brasileira de Pesquisa Agropecuária)
Usa CRISPR para desenvolver variedades de soja, milho e feijão com maior resistência a pragas e tolerância à seca.
Trabalha também em edição genética de bovinos para resistência a doenças e maior produtividade.
Universidade de São Paulo (USP)
Pesquisas com CRISPR para corrigir mutações associadas a doenças raras (ex.: Distrofia muscular de Duchenne e Fibrose cística) em modelos animais e células humanas.
Desenvolvimento de ferramentas CRISPR customizadas para laboratórios brasileiros, reduzindo custo de importação.
Universidade Estadual de Campinas (Unicamp)
Estuda uso de CRISPR em leveduras para produção de biocombustíveis e em plantas de cana-de-açúcar para aumento de produtividade.
Pesquisas em biofármacos e terapias celulares.
Fiocruz (Fundação Oswaldo Cruz)
Aplicações em saúde pública, como desenvolvimento de mosquitos geneticamente modificados resistentes a Dengue e Zika.
Estudos sobre vacinas baseadas em CRISPR.
Regulação e políticas públicas
A Comissão Técnica Nacional de Biossegurança (CTNBio) autoriza pesquisas e liberações de organismos editados por CRISPR, tratando-os de forma diferente dos transgênicos tradicionais (OGMs com DNA exógeno).
Desde 2018, o Brasil é um dos poucos países que permite comercialização de produtos agrícolas editados por CRISPR, desde que não contenham genes de outras espécies.
Ainda não há aprovação de terapias humanas com CRISPR no país, mas há protocolos submetidos para avaliação pela Agência Nacional de Vigilância Sanitária (Anvisa).
Startups e iniciativas emergentes
Algumas startups brasileiras em biotecnologia já utilizam CRISPR para melhorar fermentações industriais, desenvolver bioinsumos agrícolas e enzimas personalizadas.
Há também um movimento crescente de biohackers e laboratórios comunitários, como o Garoa Hacker Clube (SP), promovendo educação em biotecnologia e edição genética.
Como ganhar dinheiro com isso hoje:
1. Terapias e produtos de saúde (alta complexidade)
Como funciona
Desenvolver terapias celulares ou genéticas usando CRISPR para doenças raras ou crônicas (ex.: Anemia falciforme, Diabetes tipo 1, Hepatite B).
Criar kits de diagnóstico molecular baseados em CRISPR (rápidos, portáteis, baratos).
Fontes de receita
Venda de terapias personalizadas (muito alto ticket, US$ 500 mil–2 mi por paciente).
Licenciamento da propriedade intelectual (patentes).
Parcerias com farmacêuticas globais.
Exemplos reais
Excision BioTherapeutics, Verve Therapeutics, Intellia Therapeutics.
No Brasil, a USP e a Fiocruz têm pesquisas prontas para spin-offs.
2. Biotecnologia agrícola (baixo risco regulatório no Brasil)
Como funciona
Usar CRISPR para criar plantas resistentes a seca, pragas e doenças, com melhor valor nutricional.
Desenvolver bioinsumos (microrganismos editados que melhoram solo e produtividade).
Fontes de receita
Venda direta de sementes, mudas ou bioinsumos.
Licenciamento da tecnologia para grandes agroindústrias.
Parcerias com cooperativas e programas de inovação (ex.: Embrapa, Sebrae, BNDES).
Vantagem estratégica no Brasil
A Comissão Técnica Nacional de Biossegurança (CTNBio) não exige registro como OGM para produtos editados por CRISPR que não inserem genes de outras espécies — o que reduz custo e tempo de mercado.
3. Plataformas, ferramentas e serviços B2B
Como funciona
Criar serviços de design de RNA-guia, vetores, linhagens celulares e análises off-target para laboratórios e empresas.
Oferecer CRISPR como “serviço sob demanda” para empresas de pesquisa, farmacêuticas, universidades.
Fontes de receita
Assinaturas SaaS, venda de reagentes personalizados, contratos de P&D.
Modelos de royalties por uso de tecnologia desenvolvida.
Exemplos
Synthego, Benchling, Twist Bioscience.
4. Educação, conteúdo e formação
Como funciona
Criar cursos, certificações, workshops e conteúdos sobre CRISPR e biotecnologia para profissionais, investidores e público leigo.
Monetizar com cursos pagos, patrocínios e plataformas de ensino.
Mercado
Explodindo: há escassez de mão de obra em edição genética.
Grande espaço para criadores independentes, laboratórios comunitários e hubs de inovação.
5. Investimento estratégico
Como funciona
Investir em startups internacionais de CRISPR (via venture capital, bolsas, crowdfunding biotech).
Criar um fundo temático ou veículo de coinvestimento com foco em biotecnologia e gene editing.
Tese
Setor com crescimento anual >20% e múltiplos altos.
Possibilidade de saída por aquisição por big pharmas (como a compra da Verve Therapeutics pela Eli Lilly por até US$ 1,3 bi em 2025).
Insight estratégico final
O Brasil tem grande vantagem competitiva em agro, biodiversidade e custo de P&D — o caminho mais rápido para ganhar dinheiro aqui costuma ser começar com aplicações agrícolas ou serviços B2B, e usar isso como trampolim para depois escalar para terapias humanas, que exigem mais capital e regulação.
O que vem pela frente
O grande desafio agora é transformar o potencial do CRISPR em tratamentos acessíveis, seguros e escaláveis. As terapias atuais ainda são caras (podem ultrapassar US$ 2 milhões por paciente), complexas e limitadas a poucos centros de excelência.
Ao mesmo tempo, surgem debates éticos sobre edição da linhagem germinativa humana (que passa para os descendentes) e sobre o uso de CRISPR em ecossistemas (como mosquitos modificados para conter doenças).
Mesmo assim, a velocidade dos avanços indica que o CRISPR está deixando de ser uma promessa e tornando-se parte concreta da medicina do século 21.
CRISPR em 2035 — O Futuro da Edição Genética
1. Medicina: terapias genéticas como rotina hospitalar
Tratamentos baseados em CRISPR serão rotina para dezenas de doenças comuns: Diabetes tipo 1, Doença de Alzheimer, Câncer e doenças cardiovasculares.
Hospitais terão plataformas de edição sob demanda, usando bibliotecas prontas de RNAs-guia para corrigir mutações específicas de cada paciente em poucos dias.
Custos cairão drasticamente (de milhões para milhares de dólares por tratamento), graças à automação de laboratórios, IA e fabricação celular em larga escala.
Surgirão seguros de saúde genéticos, com cobertura diferenciada para quem fizer “reparos preventivos” no genoma.
2. Agricultura e bioprodutos: o novo padrão
A maioria das sementes comerciais será editada por CRISPR — resistentes a seca, calor, pragas e com maior valor nutricional.
Plantas industriais (cana, milho, eucalipto) serão redesenhadas para produzir moléculas de alto valor (plásticos biodegradáveis, biocombustíveis, fármacos).
A Amazônia será alvo central de disputas globais: países e empresas tentando patentear genes da biodiversidade local via edição genética.
3. Humanos “melhorados” e tensões éticas
A edição germinativa (embriões) começará a ser autorizada em países como China e Singapura, criando os primeiros “humanos geneticamente otimizados” — com resistência a doenças e traços cognitivos ou físicos selecionados.
Isso deve gerar um mercado bilionário de “enhancement” genético privado, além de forte desigualdade social e disputas regulatórias internacionais.
Países que proibirem poderão sofrer “fuga genética de cérebros”: famílias ricas indo ao exterior para editar os filhos antes do nascimento.
⚖️ 4. Regulação, riscos e conflitos geopolíticos
Haverá acordos globais para limitar gene drives (edição que se espalha automaticamente em populações) após alguns acidentes ambientais.
O CRISPR será incluído em tratados de controle de armas biológicas, depois de tentativas de uso ofensivo por atores estatais e terroristas.
Disputas por patentes sobre genes humanos e da biodiversidade se tornarão guerras comerciais, com ações em tribunais internacionais e sanções econômicas.
5. Economia da edição genética
Empresas CRISPR estarão entre as mais valiosas do planeta, com capitalizações trilionárias, integrando saúde, agricultura e biotecnologia industrial.
Bolsas globais terão índices exclusivos de bioengenharia, e haverá fundos de investimento genômico populares entre pessoas físicas.
Surgirá um mercado paralelo de edições não regulamentadas (biohacking de performance, estética, cognição), com clínicas clandestinas em hubs tecnológicos.
“Em 2035, editar o genoma será tão banal quanto editar um documento no computador , e tão geopolítico quanto controlar petróleo.”
Quer saber mais e estar sempre na frete de outras pessoas?
Siga Tech Gossip!!!
#CRISPR #GeneEditing #Biotech #SyntheticBiology #GenomicRevolution #PrecisionMedicine #FutureOfMedicine